Varme
Varme er en overførsel af energi mellem et system og dets omgivelser, som skyldes en temperaturforskel.
Det er en af de to måder, et system kan udveksle energi med dets omgivelser på (den anden er arbejde). Hvis systemets temperatur er højere end dets omgivelser, mister det energi; hvis temperaturen er lavere, får det tilført energi. Man plejer at regne varmeoverførsler for positive når de flyder ind i systemet.
Denne definition af varme fortæller ikke noget om hvad mekanismen bag varmeoverførslen rent faktisk er. Fysisk set er varme en udveksling af energi i form af uordnet bevægelse af molekyler. Dette kan ske på flere forskellige måder. Normalt skelner man mellem tre slags varmeoverførsel: ledning, konvektion og stråling.
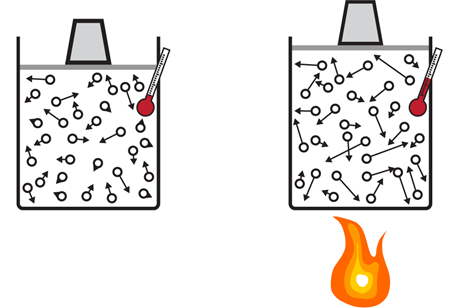
Varmeledning foregår når to genstande er i kontakt med hinanden og de har forskellig temperatur. Varmen bliver overført ved at nabomolekyler skubber til hinanden eller støder sammen. Molekylerne i den varmere genstand har i gennemsnit en højere kinetisk energi og kan overføre en del af den energi til molekylerne i den koldere genstand gennem tilfældige sammenstød. På den måde overføres varmen fra høje temperaturer til lave temperaturer; varmeledningen stopper når de to genstande har samme temperatur.
Der sker også varmeledning inden i en enkelt genstand som ikke har samme temperatur over det hele, fx en jernstang der opvarmes i den ene ende. Mængden af varme der overføres afhænger stangens materialeegenskaber og af temperaturgradienten.
Konvektion optræder i væsker (eller luftarter) i bevægelse når en del af væsken med høj temperatur strømmer ind i et område med lav temperatur. Et eksempel er en gryde med vand der opvarmes nedefra: Når det nederste lag af vand er blevet opvarmet tilstrækkeligt, vil dets opdrift få det til at stige til vejrs og skabe en konvektiv strømning. I modsætning til varmeledning er konvektiv varmetransport altid ledsaget af en overførsel af masse.
Stråling er overførsel af varme vha. elektromagnetiske bølger. Alle genstande udsender elektromagnetisk stråling (såkaldt varmestråling) pga. den tilfældige mikroskropiske bevægelse af deres molekyler som jo består af elektrisk ladede partikler. Den samlede mængde varme der udstråles fra en genstand, er proportional med dens temperatur (målt i kelvin) i fjerde potens. Hvis genstandens omgivelser har samme temperatur som den selv, vil den modtage lige så meget varmestråling som den udsender, og der vil samlet set ikke være nogen varmeoverførsel.
Omdannelse af varme til arbejde
Hvis man opvarmer en gasart der er lukket inde i en beholder, vil dens tryk stige. Trykforskellen mellem gassen og atmosfæren kan bruges til at få et stempel til at bevæge sig og dermed udføre et arbejde, fx ved at løfte et lod mod tyngdekraften..
Hvis man sammenligner den varmemængde der tilføres gassen, med det arbejde den har udført på loddet, vil arbejdet altid være mindre (noget af varmen er gået til at øge gassens temperatur, dvs. indre energi).
Det er et eksempel på en af termodynamikkens vigtigste love: Der findes ingen processer hvis eneste virkning er at omdanne varme (eller indre energi) fuldstændigt til arbejde. Derimod kan arbejde omdannes fuldstændigt til varme. Det sker fx når friktion bremser en klods der glider hen langs gulvet, eller når en elektrisk modstand bliver varm som følge af den strøm der løber i den.
Denne fundamentale asymmetri mellem varme og arbejde er et udtryk for at energien knyttet til uordnet molekylær bevægelse ikke kan omdannes fuldstændigt til makroskopisk energi knyttet til en ordnet bevægelse.